Libéthénite
La libéthénite est un minéral composé de phosphate de cuivre hydraté de formule Cu 2 PO 4. Elle est membre du groupe de l'olivénite.
|
Catégorie VIII : phosphates, arséniates, vanadates |
|||
|---|---|---|---|
|
|
|||
|
|
|||
| Formule brute | Cu2PO4 (OH) | ||
|
|
|||
| Couleur | vert olive foncé | ||
| Classe cristalline et groupe d'espace | dipyramidale, Pnnm | ||
| Système cristallin | orthorhombique | ||
| Échelle de Mohs | 4 | ||
|
|
|||
|
|
|||
| Densité | 3, 6-3, 8 | ||
|
|
|||
|
|
|||
La libéthénite est un minéral composé de phosphate de cuivre hydraté de formule Cu2PO4 (OH). Elle est membre du groupe de l'olivénite.
Elle a été trouvée au XIXe siècle au cours de l'exploitation de filons de minerais de cuivre à Libethen (Empire austro-hongrois), aujourd'hui Ľubietová en Slovaquie.
Cristallographie
La libéthénite cristallise dans le groupe d'espace orthorhombique Pnnm (Z = 4) [1].
- Paramètres de maille : a = 8, 062 Å, b = 8, 384 Å, c = 5, 881 Å ; V = 397, 51 Å3
- Densité calculée = 3, 99 g/cm3
Les cations P5+ sont en coordination tétraédrique d'anions O2– avec une longueur de liaison P-O moyenne de 1, 537 Å.
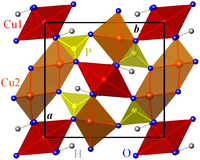
Les cations Cu2+ sont distribués sur deux sites non-équivalents : Cu1 et Cu2. Cu1 est en coordination (2+4) octaédrique déformée d'O2– et de groupes hydroxyles OH avec quatre liaisons Cu1-O courtes (longueur de liaison moyenne 1, 971 Å) et deux liaisons Cu1-O longues (2, 394 Å). Cette distribution des longueurs de liaison dans les octaèdres Cu1O4 (OH) 2 est typique de l'effet Jahn-Teller rencontré dans les composés de Cu (II) et permet une description alternative de la structure en termes de groupes plans carrés Cu1O2 (OH) 4. Cu2 est en coordination (4+1) trigonale bipyramidale déformée d'O2– et d'OH avec une longueur de liaison Cu2-O moyenne de 2, 002 Å.
Les groupes Cu1O2 (OH) 4 sont reliés entre eux par leurs arêtes et forment des chaînes CuO (OH) le long de la direction c. Les groupes Cu2O4 (OH) sont reliés par une arête et forment des dimères Cu2O6 (OH) 2 ; ils sont reliés aux chaînes CuO (OH) par un groupe hydroxyle des plans carrés Cu1O2 (OH) 4 et , plus faiblement, par un atome d'oxygène formant les liaisons longues des octaèdres Cu1O4 (OH) 2.
Propriétés
- La libéthénite agit comme un puissant catalysateur dans les réactions d'oxydo-réduction[2].
- À partir de 500 °C, la libéthénite montre des signes de déshydratation ; surtout, son cœfficient de dilatation thermique le long de la direction c devient négatif. Au dessus de 580 °C, la libéthénite est entièrement décomposée en Cu4 (PO4) 2O + H2O[2], [3].
- En-dessous de 110 K, la libéthénite présente un gap de spin : les moments magnétiques des ions Cu2+ ne sont pas ordonnés dans l'état essentiel, même à proximité du zéro absolu. Les interactions magnétiques dominantes sont celles entre les dimères Cu2O6 (OH) 2 et les chaînes CuO (OH) [4].
Notes et références
- ICSD No. 200 422 ; (en) A. Cordsen, «A crystal-structure refinement of libethenite», dans The Canadian Mineralogist, vol. 16, no 2, 1978, p. 153-157
- (en) F. -S. Xiao, J. Sun, X. Meng, R. Yu, H. Yuan, J. Xu, T. Song, D. Jiang et R. Xu, «Synthesis and structure of copper hydroxyphospate and its high catalytic activity in hydroxylation of phenol by H2O2», dans Journal of Catalysis, vol. 199, no 2, 2001, p. 273-281 [ lien DOI ]
- (en) M. Zema, S. C. Tarantino et A. M. Callegari, «Thermal behaviour of libethenite from room temperature up to dehydration», dans Mineralogical Magazine , vol. 74, no 3, 2010, p. 553-565 [ lien DOI ]
- (en) A. A. Belik, H. -J. Koo, M. -H. Whangbo, N. Tsujii, P. Naumov et E. Takayama-Muromachi, «Magnetic properties of synthetic libethenite Cu2PO4OH : a new spin-gap system», dans Inorganic Chemistry, vol. 46, no 21, 2007, p. 8684-8689 [ lien DOI ]
Recherche sur Google Images : |

"Libéthénite" L'image ci-contre est extraite du site fr.wikipedia.org Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (242 × 203 - 23 ko - jpg)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 09/12/2010.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.



 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité